Análisis completo del proceso de fabricación de fármacos de ARNm: cómo la tecnología TFF resuelve los desafíos de purificación
En los últimos años, la tecnología de ARNm ha logrado avances revolucionarios en el campo biofarmacéutico, demostrando un enorme potencial de aplicación, particularmente en vacunas y terapia génica. El exitoso desarrollo de vacunas de ARNm no sólo ha proporcionado nuevas soluciones para la prevención y el control de enfermedades infecciosas, sino que también ha impulsado avances en la inmunoterapia del cáncer y la medicina personalizada. Como clase novedosa de productos terapéuticos, la fabricación de ARNm a gran-escala es un gran desafío, ya que implica el control de la estabilidad del ARN, la eliminación de enzimas residuales y subproductos de reacción-, el intercambio de tampones y el logro de altas-tasas de recuperación de pureza, todo lo cual requiere tecnologías de fabricación con soluciones aprobadas-regulativamente.
El proceso de fabricación de vacunas o productos terapéuticos de ARNm se divide principalmente en tres etapas: preparación de una solución a granel de ADN plasmídico, preparación de una solución a granel de ARNm y preparación de un medicamento de ARNm-LNP.
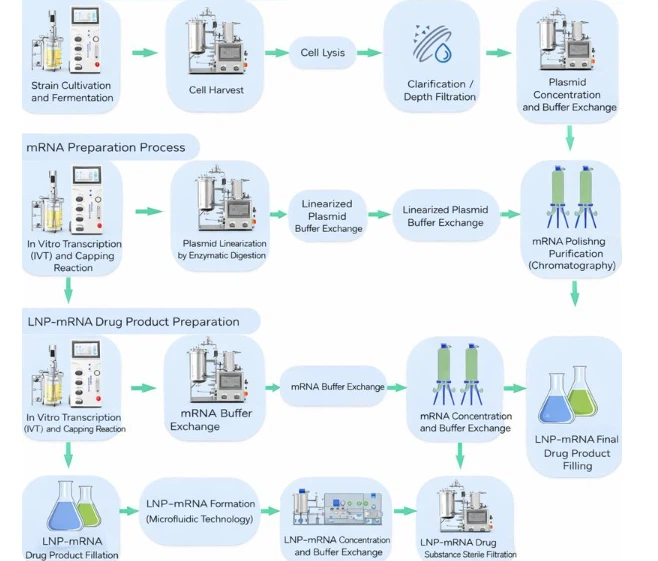
Diagrama de flujo del proceso de fabricación de medicamentos de ARNm
La filtración de flujo tangencial (TFF), como-tecnología de separación por membranas bien establecida, se aplica ampliamente en la fabricación de ARNm debido a su capacidad de tamizado molecular de alta-eficiencia, intercambio de tampón controlable y características de baja tensión de corte. Según el diseño del módulo de membrana, las configuraciones TFF comunes incluyen casetes de hoja plana-y módulos de fibra hueca-. Además, la separación de membranas impulsada por presión-en TFF se puede clasificar en microfiltración (MF), ultrafiltración (UF), nanofiltración (NF) y ósmosis inversa (RO) según el tamaño de los poros de la membrana, con una selectividad progresivamente mayor.
TFF desempeña un papel fundamental en múltiples etapas de la fabricación de fármacos de ARNm, incluida la preparación de ADN plasmídico en masa, la producción en masa de ARNm y la formulación final de productos farmacéuticos de ARNm-LNP. Mediante la selección adecuada del tipo de membrana, el límite de peso molecular-(MWCO) y el material de la membrana, TFF permite la eliminación eficiente de los subproductos-de reacción y las impurezas de bajo-peso molecular-, al mismo tiempo que facilita el intercambio y la concentración del tampón antes y después de la encapsulación de LNP. Esto mejora significativamente la pureza, la estabilidad y la escalabilidad general del proceso del ARN.
Además, el rendimiento de la filtración de flujo tangencial está influenciado por factores de configuración del sistema, como el tipo de bomba y el diseño de la tubería, así como por parámetros clave del proceso, incluida la presión transmembrana (TMP), el esfuerzo cortante y el flujo de filtración. Estos factores deben seleccionarse y optimizarse cuidadosamente en función de las características del producto objetivo, en particular para productos-sensibles al estrés, como el ARNm-LNP, que son altamente susceptibles a fuerzas mecánicas externas durante el procesamiento.
Purificación de ADN plásmido.
La preparación de una solución madre de ADN plasmídico se basa fundamentalmente en el diseño de secuencia del molde de transcripción. Los métodos de preparación suelen implicar la amplificación del ADN plasmídico, aunque también se puede utilizar la amplificación por PCR. Tomando como ejemplo la amplificación de ADN, diseñadaEscherichia colise utiliza comúnmente para la amplificación basada en-fermentación. El proceso de purificación posterior incluye principalmente recolección de células, lisis y clarificación, concentración e intercambio de tampón, filtración estéril, linealización y purificación cromatográfica. En entornos industriales, la centrifugación de flujo-continuo se utiliza a menudo para la recolección de células, pero genera fuerzas de corte relativamente altas. Los sistemas de fibras huecas, con sus canales abiertos y bajo cizallamiento, son más adecuados para manipular muestras con alto contenido de sólidos, alta viscosidad o sensibilidad al cizallamiento, como el ADN plasmídico. Después de la recolección, las células se someten a homogeneización a alta-presión, ultrasonicación o lisis alcalina, seguidas de una clarificación preliminar mediante filtración profunda.
Para facilitar la cromatografía posterior, a menudo se emplea primero la filtración de flujo tangencial (TFF) usando casetes de membrana o columnas de fibra hueca con límites de peso molecular-de 30 kDa, 100 kDa o 300 kDa para la concentración y el intercambio de tampón. Esto reduce el volumen de la muestra y al mismo tiempo elimina algunas impurezas como el ARN, las proteínas de la célula huésped (HCP) y los fragmentos de ADN de la célula huésped (HCD). La cromatografía sirve como paso de purificación central. Normalmente, la cromatografía de intercambio aniónico (AEX) se combina con la cromatografía de interacción hidrófoba (HIC) para eliminar eficazmente las impurezas y enriquecer el ADN plasmídico superenrollado altamente bioactivo, mejorando así significativamente la pureza del plásmido.
Después de la purificación, el plásmido se somete nuevamente a TFF para concentrar la solución a la concentración objetivo (generalmente 0,5 a 2 mg/ml) y realizar la diálisis con el tampón de almacenamiento final. Este paso elimina las sales residuales y los disolventes orgánicos del proceso, lo que garantiza que el sistema tampón cumpla con los requisitos para las reacciones de transcripción in vitro (IVT) posteriores.
Purificación de ARNm transcrito in vitro (IVT)
La transcripción y modificación in vitro (IVT) son los procesos clave para la preparación de soluciones madre de ARNm. Durante la producción de ARNm de IVT, se emplea una combinación de filtración de flujo tangencial (TFF1), cromatografía y filtración de flujo tangencial (TFF2). Esta estrategia garantiza una purificación eficiente y de alta-calidad del ARNm, lo que proporciona un apoyo fundamental para la fabricación de vacunas.
Una vez completadas las reacciones de transcripción y modificación, normalmente se realiza primero la ultrafiltración/diafiltración usando casetes de membrana o columnas de fibra hueca con cortes de peso molecular de 30 kDa, 100 kDa o 300 kDa. Este paso elimina eficazmente varias impurezas relacionadas con el proceso-del sistema de reacción, como la ARN polimerasa, fragmentos de ADN residuales, NTP sin reaccionar, enzimas de protección, ARN bicatenario (ARNds) e inhibidores de moléculas pequeñas-, al mismo tiempo que se logra el intercambio de tampón. Después de un único paso de filtración de flujo tangencial, la mayoría de las impurezas se eliminan eficazmente y la única impureza proteica residual detectable es la ARN polimerasa.
Posteriormente, se aplican múltiples técnicas de cromatografía para una mayor purificación. Los métodos comúnmente utilizados incluyen cromatografía de afinidad, cromatografía de exclusión-de tamaño, cromatografía de fase inversa-de pares iónicos y cromatografía de intercambio iónico-. Mediante esta combinación de ultrafiltración y cromatografía secuencial, el ARNm alcanza un alto nivel de pureza.
Para cumplir con los requisitos de formulación o almacenamiento, la solución madre de ARNm se concentra o diluye nuevamente usando casetes de membrana de 30 kDa, 100 kDa o 300 kDa o columnas de fibra hueca para ajustar con precisión la concentración objetivo y cambiarla al tampón de formulación final. Finalmente, se aplica filtración de grado estéril-para controlar la carga microbiana, completando el almacenamiento temporal y el llenado del material.
Exploration of TFF-related process parameters: Relevant studies have shown that a membrane with a molecular weight cut-off (MWCO) of 100 kDa provides the optimal purification efficiency; the transmembrane pressure (TMP) should not exceed 5 psi; and an mRNA concentration of 1 mg/mL ensures a relatively high permeate flux (>25LMH).
Purificación de formulaciones de ARNm-LNP
Las nanopartículas lipídicas (LNP) son actualmente el sistema de administración más estudiado para terapias con ARNm. En la actualidad, varias formulaciones de ARNm-LNP se encuentran en diferentes etapas de desarrollo preclínico y clínico. Los LNP son muy sensibles a los procesos de fabricación. Entre las operaciones unitarias necesarias para la producción de ARNm-LNP, la concentración y el intercambio de tampón mediante filtración de flujo tangencial (TFF), así como la filtración estéril, presentan desafíos importantes. Estos pasos deben optimizarse cuidadosamente para garantizar la escalabilidad del proceso y la calidad del producto, evitando al mismo tiempo problemas como la contaminación de las membranas y la carga incorrecta del filtro.
Después de la encapsulación del ARNm, se utiliza filtración de flujo tangencial (TFF) para la purificación. El propósito de este paso es eliminar el ARNm no encapsulado, los polímeros libres o los materiales lipídicos, así como los disolventes residuales del ARNm y los lípidos. Dado que los LNP de ARNm-exhiben una estabilidad limitada a temperatura ambiente, la optimización de los procesos posteriores, incluido el TFF, es fundamental para mantener la calidad del producto.
Las direcciones clave de optimización incluyen: establecer adecuadamente la presión transmembrana (TMP) y el caudal tangencial en función del tamaño de las partículas y la estabilidad de los ARNm-LNP para equilibrar la eficiencia de la filtración y el estrés de las partículas; seleccionar membranas o columnas de fibra hueca con límites de peso molecular adecuados-(MWCO, por ejemplo, 100 kDa o 300 kDa) para eliminar eficazmente el ARNm libre, las impurezas y el tampón de intercambio mientras se minimiza la adsorción o el daño de partículas; y optimizar los volúmenes de concentración y diafiltración para garantizar un intercambio eficaz de tampón en la formulación objetivo y controlar la concentración y dispersidad final de las partículas.
Además, los atributos de calidad críticos (como el tamaño de partícula, el índice de polidispersidad [PDI] y la eficiencia de encapsulación de ARNm) se deben monitorear de cerca durante el proceso, y los parámetros se deben ajustar dinámicamente en función de datos en tiempo real-para lograr una purificación y formulación estable, escalable y eficiente de ARNm-LNP.
Además, debido a la inestabilidad de los LNP de ARNm-y sus componentes bajo métodos de esterilización terminal, normalmente se utiliza un filtro de grado estéril- de 0,2 µm para eliminar bacterias y otros contaminantes microbianos.

